RSV-Infektionen
Präambel
Die Herausgabe der RKI-Ratgeber erfolgt durch das Robert Koch-Institut (RKI) auf der Grundlage des § 4 Infektionsschutzgesetz (IfSG). Zielgruppe der RKI-Ratgeber sind Fachkreise, u.a. Ärztinnen und Ärzte, medizinisches Fachpersonal und der öffentliche Gesundheitsdienst (ÖGD). Informationen zu wichtigen Infektionskrankheiten sollen aktuell und konzentriert der Orientierung dienen. Die Beiträge werden in Zusammenarbeit mit den Nationalen Referenzzentren (NRZ), Konsiliarlaboren (KL) sowie weiteren Expertinnen und Experten erarbeitet. Die RKI-Ratgeber sind auf der Internetseite des RKI (www.rki.de/ratgeber) abrufbar. Neu erstellte RKI-Ratgeber und deutlich überarbeitete Folgeversionen werden im Epidemiologischen Bulletin (www.rki.de/epidbull) veröffentlicht.
Erstveröffentlichung im Epidemiologischen Bulletin 03/2004.
Vollständig aktualisierte Fassung, veröffentlicht im Epidemiologischen Bulletin 1/2024.
Letzte Aktualisierung:
- Kapitel „Primärpräventive Maßnahmen“ (August 2024)
Erreger
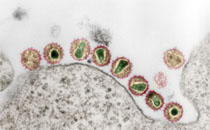
Das Respiratorische Synzytial-Virus (RSV) ist ein einzelsträngiges, negativ orientiertes, unsegmentiertes RNA-Virus aus der Familie der Pneumoviridae (Genus Orthopneumovirus). Das Genom hat eine Größe von 15 Kilobasen und kodiert für 10 Gene. RSV besitzt eine doppelschichtige Lipidhülle, in die Glykoproteine eingelagert sind, darunter ein Fusions-(F-) und ein Adhäsions-(G-)Protein. Es gibt zwei Gruppen von RSV, A und B, die sich in der Antigenstruktur des G-Proteins unterscheiden. Virusstämme beider Gruppen zirkulieren gleichzeitig, RSV A dominiert jedoch in den meisten Jahren.
Vorkommen
Das RSV ist ein weltweit verbreiteter Erreger von akuten Erkrankungen der oberen und unteren Atemwege in jedem Lebensalter und einer der bedeutendsten Erreger von Atemwegsinfektionen bei Säuglingen, insbesondere Frühgeborenen, Kleinkindern sowie älteren Erwachsenen. In Saisonalität und Symptomatik ähneln RSV-Infektionen der Influenza. Ihre Verbreitung in der Allgemeinbevölkerung wurde lange Zeit unterbewertet. Nach aktuellen Schätzungen kommen RSV-assoziierte akute untere Atemwegserkrankungen jedoch weltweit jährlich mit einer Inzidenz von rund 95 Fällen und 16 hospitalisierten Fällen pro 1.000 Kindern im 1. Lebensjahr vor. In einer Übersichtsarbeit zur Letalität schwerer RSV-bedingter Erkrankungen der unteren Atemwege bei hospitalisierten Kleinkindern (≤ 2 Jahre) wurden Daten aus mehreren Primärstudien analysiert: Es zeigte sich, dass im Mittel 0,2% der Fälle bei Kindern ohne bekanntes erhöhtes Risiko, 1,2% bei Frühgeborenen, 4,1% bei Kindern mit bronchopulmonaler Dysplasie und 5,2% bei Kindern mit angeborenem Herzfehler tödlich verliefen.
Seit der Wintersaison 2010/11 berichtet das RKI über die aktuelle RSV-Situation in Deutschland (http://influenza.rki.de/). RSV-Infektionen treten zyklisch auf. Die RSV-Inzidenz ist von November/Dezember bis März/April am höchsten (RSV-Erkrankungswelle bzw. RSV-Saison), in den übrigen Monaten kommen sporadische Infektionen vor. Der Gipfel der RSV-Saison erstreckt sich über etwa 4–8 Wochen und liegt meist im Januar und Februar, seltener auch im November und Dezember.
Während der Coronavirus Disease 2019-(COVID-19-)Pandemie und den damit assoziierten Infektionsschutzmaßnahmen war das übliche saisonale Muster von RSV-Infektionen zeitlich verschoben. Eine reguläre RSV-Erkrankungswelle fehlte in der Wintersaison 2020/21 in Deutschland. Nach der Lockerung der Infektionsschutzmaßnahmen im Jahr 2021 zirkulierte RSV in Deutschland ungewöhnlich früh außerhalb des üblichen Zeitraums, von August bis Dezember. Die nachfolgende RSV-Erkrankungswelle in der Saison 2022/23 begann ebenfalls früh im Oktober und endete im Januar.
RSV-Infektionen betreffen alle Altersgruppen. Es besteht kein vollständiger Nestschutz. Neugeborene und Säuglinge können jedoch in den ersten 4–6 Lebenswochen durch diaplazentar übertragene Antikörper vor einer RSV-bedingten Erkrankung geschützt sein, während Frühgeborene durch eine geringere Versorgung mit maternalen Antikörpern auch in den ersten Lebenswochen bereits schwer an einer RSV-Infektion erkranken können. Bei älteren Säuglingen und Kleinkindern ist eine RSV-Infektion die häufigste Ursache von Erkrankungen des unteren Respirationstraktes und von damit verbundenen Krankenhauseinweisungen. Innerhalb des 1. Lebensjahres haben 50–70% und bis zum Ende des 2. Lebensjahres nahezu alle Kinder mindestens eine RSV-Infektion durchgemacht. Eine langfristige Immunität besteht nicht. Reinfektionen sind häufig, insbesondere bei Erwachsenen mit regelmäßigem Kontakt zu Kleinkindern.
RSV-Infektionen treten bei Frauen und Männern gleichermaßen auf. Schwere, mit einem Krankenhausaufenthalt verbundene RSV-bedingte Erkrankungen bei Kindern betreffen häufiger Jungen als Mädchen.
Zu den Risikogruppen, die schwer an einer RSV-Infektion erkranken können, gehören Frühgeborene, Neugeborene, Säuglinge sowie Kinder mit schweren Grunderkrankungen, vor allem mit chronischen Lungenerkrankungen (z.B. bronchopulmonale Dysplasie, interstitielle Lungenerkrankung, zystische Lungenfibrose, angeborene Atemwegsanomalien), schweren Herzerkrankungen und komplexen angeborenen Herzfehlern, angeborenen oder erworbenen Formen der schweren Immundefizienz, neuromuskulären Erkrankungen, syndromalen Erkrankungen wie Trisomie 21 und angeborenen Fehlbildungen. Zu den Risikogruppen unter Erwachsenen gehören Personen mit kardialen oder pulmonalen Vorerkrankungen sowie immundefiziente und immunsupprimierte Personen. Besonders gefährdet sind auch Empfängerinnen und Empfänger hämatopoetischer Zelltransplantate oder Lungen- oder anderer Organtransplantate sowie stark immunsupprimierte Personen mit maligner hämatologischer Erkrankung.
Nosokomiale RSV-Infektionen sind bei Frühgeborenen sowie immundefizienten und immunsupprimierten Personen bedeutsam. RSV ist einer der wichtigsten Erreger einer nosokomialen Infektion und Pneumonie bei Säuglingen und Kleinkindern.
Ein vereinfachter Datenbestand der gemäß IfSG an das RKI übermittelten RSV-Infektionen für Deutschland kann mit Hilfe von SurvStat@RKI unter www.rki.de/survstat abgefragt werden.
Reservoir
Der Mensch ist das einzige relevante Reservoir für das humane RSV.
Infektionsweg
Die Übertragung erfolgt in erster Linie durch Tröpfcheninfektion von einer infektiösen Person auf eine Kontaktperson. Die Schleimhaut der oberen Atemwege, hauptsächlich die zilientragenden Epithelzellen, und die Konjunktiven bilden die Eintrittspforten. Es wird angenommen, dass eine Übertragung auch indirekt über kontaminierte Hände, Gegenstände und Oberflächen auf die Schleimhäute der Atemwege möglich ist. RSV kann in respiratorischem Sekret 20 Minuten auf Händen infektiös bleiben, 45 Minuten auf Papierhandtüchern und Baumwollkitteln und bis zu mehreren Stunden auf Einmalhandschuhen, auf Stethoskopen und auf Kunststoffoberflächen. Jugendliche und Erwachsene spielen als asymptomatische oder symptomarme Überträger eine Rolle. Auch passiv gegen RSV immunisierte Kinder können vorübergehend Überträger von RSV sein, da die Antikörper nicht die Infektion der oberen Atemwege verhindern. Medizinisches Personal und andere Kontaktpersonen der Erkrankten können somit zu einer raschen, auch nosokomialen Ausbreitung beitragen, wenn Schutz- und Hygienemaßnahmen lückenhaft sind.
Inkubationszeit
Die Inkubationszeit beträgt 2–8 Tage (durchschnittlich 5 Tage).
Klinische Symptomatik
Eine RSV-Infektion kann das Symptomspektrum von einer einfachen Atemwegsinfektion bis zu einer schweren beatmungspflichtigen Erkrankung der unteren Atemwege zeigen oder auch asymptomatisch verlaufen.
Eine Primärinfektion mit RSV führt fast immer zu einer deutlichen klinischen Symptomatik. Die Erkrankung kann auf die oberen Atemwege beschränkt sein, sich aber auch, insbesondere bei Säuglingen in den ersten Lebensmonaten, als Bronchiolitis, Pneumonie oder Tracheobronchitis äußern. Ein keuchhustenähnliches Krankheitsbild kommt bei etwa 5% der Fälle mit Beteiligung der unteren Atemwege vor. Fieber ist bei Kindern häufig und tritt auch bei leichteren Verläufen auf. Im Krankheitsverlauf werden in der Regel zuerst Symptome einer Erkrankung der oberen Atemwege (Schnupfen, nichtproduktiver Husten, eventuell Pharyngitis) beobachtet, die innerhalb von 1–3 Tagen zu Symptomen einer unteren Atemwegserkrankung fortschreiten können. Meist wird der Husten hierbei deutlicher und produktiver, die Atemfrequenz steigt und es kann zu einer Dyspnoe kommen. Zeichen einer exspiratorischen Obstruktion sind typisch. Die RSV-Bronchiolitis bei Säuglingen ist gekennzeichnet durch einen reduzierten Allgemeinzustand, Schwierigkeiten bei der Nahrungsaufnahme (Trinkschwäche, Reflux, Erbrechen), beschleunigte Atmung, Husten und Dyspnoe.
Über den Lungen sind sowohl knisternde als auch giemende Geräusche auskultierbar. Während bei der Bronchiolitis das exspiratorische Giemen im Vordergrund steht, kann es bei schwerem Verlauf auch zu einer „stillen Obstruktion“ mit Tachypnoe und verringerter peripherer Durchblutung kommen. Eine Verengung der Atemwege, schlecht belüftete (Atelektasen betreffen typischerweise den rechten Lungenoberlappen) und kompensatorisch überbelüftete Lungenareale und ein niedriges Ventilations-Perfusions-Verhältnis können zu Hyperkapnie und Hypoxämie führen. Bei Frühgeborenen sind rezidivierende Apnoen charakteristisch. Die Symptomatik kann im Einzelfall sehr unterschiedlich ausgeprägt sein. Schnelle Veränderungen des klinischen Zustandes sind möglich, weshalb engmaschige Untersuchungen wichtig sind.
RSV-Reinfektionen sind häufig und kommen in jedem Lebensalter vor. Bei Kindern kommt es auch bei Reinfektion häufig zu Erkrankungen der unteren Atemwege, die jedoch meist weniger schwer als bei der Primärinfektion verlaufen. Meist dauert die Erkrankung etwa 3–12 Tage, wobei respiratorische Symptome, insbesondere Husten, über mehr als 4 Wochen anhalten können. Bei Erwachsenen verlaufen RSV-Reinfektionen oft asymptomatisch oder als unkomplizierte Infektion der oberen Atemwege.
Komplikationen einer RSV-Infektion treten insbesondere bei Risikogruppen (s. Abschnitt „Vorkommen“) auf. Bei Patientinnen und Patienten aller Altersgruppen mit chronischen pulmonalen und kardialen Vorerkrankungen, mit Asthma bronchiale und mit schweren neurologischen Erkrankungen kommt es häufig zu einer Exazerbation der vorbestehenden Erkrankung. Diese Patientinnen und Patienten sowie immundefiziente und immunsupprimierte Personen haben ein besonderes Risiko, an einer schweren RSV-bedingten Pneumonie zu erkranken.
Sekundäre bakterielle Infektionen kommen bei RSV-Infektionen eher selten vor, Koinfektionen mit anderen respiratorischen Viren sind häufig.
Eine häufige Komplikation einer RSV-Infektion ist eine akute Otitis media. Vor allem bei Kindern unter 3 Jahren wird RSV häufig allein oder als Koinfektion mit anderen viralen oder bakteriellen Erregern nachgewiesen.
Als Langzeitkomplikation einer akuten RSV-induzierten Bronchiolitis sind wiederkehrende Obstruktionen und eine anhaltende Hyperreagibilität des Bronchialsystems beschrieben.
Dauer der Ansteckungsfähigkeit
RSV-Infizierte können schon einen Tag nach der Ansteckung und noch vor Symptombeginn infektiös sein. Die Dauer der Ansteckungsfähigkeit beträgt in der Regel 3–8 Tage und klingt bei immunkompetenten Personen meist innerhalb einer Woche ab. Frühgeborene, Neugeborene, immundefiziente oder immunsupprimierte Personen können das Virus über mehrere Wochen, im Einzelfall über Monate ausscheiden.
Diagnostik
Das klinische Bild und das Lebensalter können einen Hinweis auf eine RSV-Infektion geben, zur Sicherung der Diagnose bedarf es jedoch eines Erregernachweises. Dieser sollte zeitnah erfolgen, um nosokomialen RSV-Infektionen wirksam vorzubeugen und therapeutische Entscheidungen zu treffen. Wie für andere virale Erreger von Atemwegserkrankungen eignet sich Nasopharyngealsekret aus Nasenrachenabstrichen, -aspiration oder -spülwasser für den Nachweis von RSV.
1. Differenzialdiagnostik
Da viele andere Atemwegserreger, wie z.B. humane Metapneumoviren, Influenzaviren oder das Severe Acute Respiratory Syndrome Coronavirus Type 2 (SARS-CoV-2) sehr ähnliche klinische Bilder hervorrufen können wie RSV, kann letztendlich eine sichere Abgrenzung nur durch eine Labordiagnostik erfolgen. Insbesondere bei Säuglingen und Kleinkindern sollte bei akuten respiratorischen Symptomen während der Hochphase einer RSV-Erkrankungswelle an eine RSV-Infektion gedacht werden.
2. Labordiagnostik
Genomnachweise mittels Polymerasekettenreaktion (PCR) sind selbst bei geringer Viruslast in der Probe sehr spezifisch, schnell und hochsensitiv. Zur Verfügung stehen RSV-spezifische PCR-Nachweissysteme sowie Multiplex-PCR zum parallelen Nachweis von RSV und anderen Erregern von Atemwegsinfektionen. Einige der verfügbaren PCR-Systeme können RSV-positive Proben zusätzlich in die RSV-Gruppen A und B differenzieren.
Als Antigennachweis sind Schnelltests verfügbar, die RSV allein oder in Kombination mit anderen Erregern (SARS-CoV-2, Influenza A/B) nachweisen. Generell ist die Sensitivität von RSV-Antigenschnelltests mit etwa 74% deutlich niedriger als bei der PCR, die Spezifität ist mit 98% dagegen zumeist hoch. Generell gibt es große Unterschiede bei der Sensitivität und Spezifität der Tests verschiedener Anbieter. Der positive Vorhersagewert hängt stark vom Alter der Erkrankten und der epidemiologischen Situation ab. Bei Säuglingen und Kleinkindern während der RSV-Saison ist die diagnostische Aussagekraft deutlich höher als bei älteren Kindern, Erwachsenen (inklusive älteren und immungeschwächten Personen) oder der Testdurchführung außerhalb der Saison.
Die Viruskultur spielt für die Routinediagnostik keine Rolle mehr und wird hauptsächlich von Speziallaboratorien oder im Rahmen von Studien durchgeführt.
Antikörpernachweise sind im Vergleich zu direkten Erregernachweisen von untergeordneter Bedeutung. Bei einer RSV-Infektion werden Antikörper nur in geringfügiger Konzentration gebildet. Um einen Titeranstieg zu erfassen, müssen zwei Seren mit mindestens 2–4 Wochen Abstand untersucht werden. Antikörpernachweise sind daher vor allem zur retrospektiven Sicherung der Diagnose und zu Forschungszwecken geeignet.
Therapie
Eine wirksame kausale Behandlung der RSV-Infektion existiert nicht. Die Therapie erfolgt symptomatisch und besteht in ausreichender Flüssigkeitszufuhr zur Sekretmobilisation und Freihalten des Nasopharynx mit NaCl-Nasenspülungen oder -tropfen.
Abhängig vom individuellen Gesundheitszustand der Patientin oder des Patienten können Sauerstoffgaben, Atemunterstützung mit CPAP-Maske (CPAP: continuous positive airway pressure) oder Intubation und Beatmung erforderlich werden. In einigen Fällen kann die Inhalation mit Bronchodilatatoren, insbesondere Adrenalin, die Atemnot lindern, sie beeinflusst den Verlauf einer Bronchiolitis jedoch nicht. Eine parallele Überwachung der Sauerstoffsättigung zu Beginn der Inhalationsbehandlung sollte erfolgen, da eine Hypoxämie verstärkt werden kann. Für RSV-assoziierte Apnoen gibt es keine medikamentöse Behandlung, eine stationäre Überwachung ist wichtig.
Antibiotikagaben beeinflussen weder den klinischen Verlauf einer RSV-Infektion noch die Dauer der Ansteckungsfähigkeit. Eine antibakterielle Therapie ist nur indiziert, wenn eine bakterielle Ko- oder Sekundärinfektion vorliegt. Wichtig ist daher ein sorgfältiges Monitoring auf Anzeichen einer bakteriellen Infektion, wie z.B. eine sekundäre klinische Verschlechterung.
Infektionsschutz und Hygienemaßnahmen
1. Primärpräventive Maßnahmen
Eine gänzliche Vermeidung von RSV-Infektionen im Alltag ist schwierig. Zu den Maßnahmen zur Vermeidung schwerer Krankheitsverläufe und der Ausbreitung von RSV-Infektionen gehören eine zeitnahe Diagnostik sowie Hygienemaßnahmen für Patientinnen und Patienten, Personal und Kontaktpersonen. Das konsequente Einhalten von Hygienemaßnahmen zur Reduktion von akuten Atemwegsinfektionen sollte befolgt werden. Außerdem stehen in Deutschland zum Schutz vor RSV-Erkrankungen für Säuglinge ein monoklonaler Antikörper, ein maternaler RSV-Impfstoff und 2 RSV-Impfstoffe für ältere Erwachsene zur Verfügung. Details zur Zulassung, zu den Anwendungshinweisen und zu den Empfehlungen folgen unten.
Zur Desinfektion sind Mittel mit nachgewiesener Wirksamkeit mit dem Wirkungsbereich „begrenzt viruzid“ (wirksam gegen behüllte Viren) anzuwenden. Mittel mit einem erweitertem Wirkbereich gegen Viren wie "begrenzt viruzid PLUS" oder "viruzid" können ebenfalls verwendet werden. Geeignete Mittel sind z.B. in der "Liste der vom RKI geprüften und anerkannten Desinfektionsmittel und -verfahren" und der Desinfektionsmittel-Liste des Verbundes für Angewandte Hygiene (VAH) enthalten. Bei behördlich angeordneten Desinfektionsmaßnahmen ist die RKI-Liste heranzuziehen.
Die Vorbeugung nosokomialer RSV-Infektionen ist eine Aufgabe mit höchster Priorität. Daher sind Hygienemaßnahmen in Krankenhäusern, Pflegeeinrichtungen und auch ambulanten ärztlichen Praxen wichtig. Medizinisches Personal sollte beim Kontakt mit Erkrankten Schutzkittel, Einmalhandschuhe und geeigneten Atemschutz tragen (hier ein direkt anliegender, mehrlagiger Mund-Nasen-Schutz), um einer Virusinokulation über die Schleimhäute und einer weiteren Virenübertragung vorzubeugen.
Weiterführende Angaben sind z.B. in der Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) "Infektionsprävention im Rahmen der Pflege und Behandlung von Patienten mit übertragbaren Krankheiten"(2015) und der assoziierten aktualisierten Tab. 1 dieser Empfehlung (2023) sowie der "Vollzugshilfe zur Entsorgung von Abfällen aus Einrichtungen des Gesundheitsdienstes" enthalten.
Für die Aspekte des Arbeitsschutzes sind die einschlägigen Technischen Regeln für biologische Arbeitsstoffe, wie z.B. die TRBA 250 zu beachten, die von der Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA) veröffentlicht werden.
RSV-Impfstoffe
Im Sommer 2023 wurden in der Europäischen Union (EU) erstmals zwei proteinbasierte RSV-Impfstoffe (Arexvy; GSK und Abrysvo; Pfizer) zum Schutz vor RSV-bedingten tiefen Atemwegsinfektionen zugelassen. Die Impfstoffe enthalten das in der Präfusionskonfirmation stabilisierte Fusionsprotein des RS-Virus (RSV-Pre-F-Protein). Die im Rahmen der Immunantwort gebildeten neutralisierenden Antikörpern gegen das RSV-Pre-F-Antigen hindern das RS-Virus an der Fusion mit der Zellmembran und somit an dem Zelleintritt. Beide Impfstoffe sind zum Schutz vor RSV bei Personen ab 60 Jahre zugelassen und Abrysvo zudem zum Schutz von Säuglingen als maternale Impfung von Schwangeren in der 24. bis 36. Schwangerschaftswoche. Beide Impfstoffe sind seit der Saison 2023/24 in Deutschland verfügbar.
RSV-Prophylaxe (Passive Immunisierung)
In der EU war bis Ende 2022 zur medikamentösen Prophylaxe von RSV-Erkrankungen der unteren Atemwege nur der monoklonale RSV-Antikörper Palivizumab (Synagis) zugelassen, der sich gegen das F-Protein von RSV richtet. Palivizumab ist ausschließlich zur RSV-Prophylaxe bei Kindern mit einem hohem Risiko für einen schweren Krankheitsverlauf zugelassen; hierzu zählen Frühgeborene und Kinder < 2 Jahre mit bronchopulmonaler Dysplasie oder mit hämodynamisch relevanten Herzerkrankungen. Palivizumab soll während der RSV-Saison (meist Oktober bis März) in monatlichen Intervallen intramuskulär verabreicht werden, wobei die Applikation der 1. Dosis vor Beginn der RSV-Saison erfolgen sollte.
Im Oktober 2022 hat die EU den monoklonalen RSV-Antikörper Nirsevimab (Beyfortus) zugelassen. Nirsevimab zeichnet sich durch eine verlängerte Halbwertszeit (ca. 69 Tage) aus und ist zur Prävention von RSV-Erkrankungen der unteren Atemwege bei Neugeborenen und Säuglingen unabhängig von bestehenden Risikofaktoren in ihrer 1. RSV-Saison zugelassen. Bei Nirsevimab handelt es sich ebenfalls um einen monoklonalen Antikörper, der sich wie Palivizumab gegen die Präfusionskonformation des RSV-F-Protein richtet und die Fusion der Zellmembran infizierter Zellen mit den Nachbarzellen hemmt und somit das Eindringen von RSV in die Zelle und ihre Ausbreitung verhindert. Nirsevimab wird als Einmaldosis von 50 mg an Säuglinge mit einem Körpergewicht < 5 kg intramuskulär verabreicht; bei einem Gewicht ≥ 5 kg beträgt die Einmaldosis 100 mg. Die Wirkung setzt unmittelbar nach der Verabreichung ein und hält über die gesamte RSV-Saison an.
Empfehlungen der Ständigen Impfkommission (STIKO)
RSV-Prophylaxe (Passive Immunisierung) für Säuglinge:
Seit Ende Juni 2024 empfiehlt die STIKO allen Neugeborenen und Säuglingen unabhängig von möglichen Risikofaktoren eine RSV-Prophylaxe mit dem monoklonalen Antikörper Nirsevimab (Beyfortus) als Einmaldosis vor bzw. in ihrer 1. RSV-Saison (Epid Bull 26/2024).
- Säuglinge, die zwischen April und September geboren sind, sollen Nirsevimab möglichst im Herbst vor Beginn ihrer 1. RSV-Saison erhalten.
- Neugeborene, die während der RSV-Saison (üblicherweise zwischen Oktober und März) geboren werden, sollen Nirsevimab möglichst rasch nach der Geburt bekommen, idealerweise bei Entlassung aus der Geburtseinrichtung bzw. bei der U2-Untersuchung (3. – 10. Lebenstag).
- Eine versäumte Nirsevimab-Gabe soll innerhalb der 1. RSV-Saison schnellstmöglich nachgeholt werden.
Ziel der STIKO-Empfehlung ist es, die Häufigkeit schwer verlaufender RSV-Erkrankungen bei Neugeborenen und Säuglingen jeglichen Gestationsalters unabhängig von möglichen Risikofaktoren in ihrer 1. RSV-Saison in Deutschland zu reduzieren. Insbesondere sollen RSV-bedingte Hospitalisierungen, intensivmedizinische Behandlungen, RSV-bedingte Todesfälle sowie stationäre und ambulante Versorgungsengpässe verhindert werden.
RSV-Impfung für Erwachsene:
Seit Anfang August empfiehlt die STIKO für alle Personen ≥ 75 Jahre eine 1-malige RSV-Impfung mit einem proteinbasierten RSV-Impfstoff (Arexvy oder Abrysvo) möglichst vor der RSV-Saison als Standardimpfung. Außerdem wird Personen im Alter von 60 bis 74 Jahren mit einer schweren Grunderkrankung oder Personen, die in einer Einrichtung der Pflege leben und somit ein deutlich erhöhtes Risiko für einen schweren RSV-Krankheitsverlauf haben, ebenfalls eine 1-malige RSV-Impfung als Indikationsimpfung empfohlen (Epid Bull 32/2024). Zu den Grunderkrankungen gehören schwere Formen von u.a. chronischen Erkrankungen der Atmungsorgane, chronischen Herz-Kreislauf- und Nierenerkrankungen, chronischen neurologischen und neuromuskulären Erkrankungen, hämato-onkologischen Erkrankungen, Diabetes mellitus (mit Komplikationen) sowie einer schweren angeborenen oder erworbenen Immundefizienz.
Auf Basis der aktuellen Datenlage kann noch keine Aussage zur Notwendigkeit von Wiederholungsimpfungen getroffen werden. Für einen optimalen Schutz in der RSV-Saison sollte die Impfung im Spätsommer/Herbst erfolgen. Die RSV-Impfung kann gleichzeitig mit der saisonalen Influenza-Impfung verabreicht werden.
Ziel der RSV-Impfempfehlung ist die Reduktion schwerer RSV-assoziierter Atemwegserkrankungen sowie der daraus resultierenden Folgen wie Hospitalisierung und Tod.
Hinsichtlich der maternalen Impfung kam die STIKO nach Prüfung der Evidenz aus den klinischen Studien zu dem Schluss, dass die Datenlage zum jetzigen Zeitpunkt nicht ausreicht, um über eine mögliche Empfehlung entscheiden zu können (Stand: August 2024).
Empfehlungen der Fachgesellschaften zur RSV-Impfung
Die Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie (DGHO) empfiehlt seit August 2023 eine RSV-Schutzimpfung bei immundefizienten Patientinnen und Patienten mit hämatologischen oder onkologischen Erkrankungen. Für die Kostenübernahme durch die Krankenkasse ist ein Antrag auf Off-Label-Use erforderlich (s. Empfehlung der DGHO).
Die Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin e. V. (DGP) empfiehlt seit November 2023 eine RSV-Impfung bei Personen im Alter von ≥ 60 Jahren. Darüber hinaus empfiehlt die DGP nach individueller Beratung die RSV-Impfung bei Erwachsenen jeden Alters mit schweren pulmonalen oder kardiovaskulären Vorerkrankungen sowie bei Erwachsenen mit einer deutlichen Einschränkung der Immunabwehr. Eine Kostenübernahme kann individuell bei der zuständigen Krankenkasse beantragt werden (s. Positionspapier der DGP).
Die pädiatrischen Fachgesellschaften empfehlen die beiden monoklonalen Antikörper (Palivizumab und Nirsevimab) bislang nur für ausgewählte pädiatrische Risikogruppen (s. AMWF-Leitlinie 048/012).
Die gynäkologischen Fachgesellschaften empfehlen die saisonale RSV-Impfung für Schwangere ab 32. SSW in informierter partizipativer Entscheidungsfindung.
2. Maßnahmen bei Einzelerkrankungen
Mit RSV infizierte Personen sind über Schutz- und Hygienemaßnahmen aufzuklären. Während der Ansteckungsfähigkeit sollten sie Gemeinschaftseinrichtungen, insbesondere Krabbelgruppen nicht besuchen, auch wenn kein explizites Tätigkeits- oder Betretungsverbot für Gemeinschaftseinrichtungen gemäß § 34 Abs. 1 und 3 IfSG besteht.
Erfolgt ein RSV-Nachweis bei einer hospitalisierten Person, sollte dieser räumlich über die gesamte Dauer der Ansteckungsfähigkeit von anderen, insbesondere von Säuglingen und Risikogruppen getrennt werden. Eine Kohortenisolierung mehrerer RSV-Infizierter ist möglich. In pädiatrischen Abteilungen und Abteilungen mit immunsupprimierten Patientinnen und Patienten sollten mit RSV infizierte Personen über die gesamte Dauer ihrer Symptomatik in Isolierzimmern behandelt werden (s. o. g. Empfehlung der KRINKO).
Umgang mit infektiösen Verstorbenen
Der Umgang mit infektiösen Verstorbenen ist in den Seuchen- und Infektionsalarmplänen, den Bestattungsgesetzen der Bundesländer und der Information 214-021 der Deutschen Gesetzlichen Unfallversicherung "Biologische Arbeitsstoffe beim Umgang mit Verstorbenen" geregelt. Erreger werden durch den Ausschuss für Biologische Arbeitsstoffe (ABAS) in Risikogruppen eingestuft. Es wird daher empfohlen, auf der Todesbescheinigung (Totenschein bzw. Leichenschauschein) die Erkrankung namentlich zu benennen. Datenschutzrechtliche Bestimmungen der Länder sind dabei zu beachten. Für in Bestattungsunternehmen tätige Personen gelten auch die arbeitsschutzrechtlichen Regelungen nach der BioStoffV. Eine individuelle Gefährdungsbeurteilung muss vor Arbeitsaufnahme durchgeführt werden, um das individuelle Infektionsrisiko abzuschätzen und entsprechende Schutzmaßnahmen ergreifen zu können. Für weitere Informationen hierzu sei hier auf die Vorgaben des Arbeitsschutzes (s. u.a. TRBA 250) und auf die Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA) und die bestattungsrechtlichen Regelungen des jeweiligen Bundeslandes verwiesen.
3. Umgang mit Kontaktpersonen
Kontaktpersonen von mit RSV infizierten Personen sind über Hygienemaßnahmen aufzuklären. Insbesondere Risikogruppen sollten nicht durch Kontakt zu Personen mit RSV- und anderen Atemwegsinfektionen gefährdet werden, z.B. durch Besuchende oder Personal mit einer akuten Atemwegssymptomatik. Eine Möglichkeit der Chemoprophylaxe für Kontaktpersonen besteht nicht.
4. Maßnahmen bei Ausbrüchen
Im Falle eines Ausbruchs in Krankenhäusern und anderen Gesundheitseinrichtungen gelten Hygienemaßnahmen gleichermaßen. Kommt es zu einem RSV-Ausbruch in Hochrisikobereichen, wie einer neonatologischen Intensivstation mit kritisch kranken Frühgeborenen oder langzeitbeatmeten Kindern mit bronchopulmonaler Dysplasie, sollten alle Risikogruppen der Abteilung in Untersuchungen einbezogen werden, um eine Erregerausbreitung frühzeitig zu erkennen und einzudämmen. Das RKI stellt eine Checkliste für das Management respiratorischer Ausbrüche in Pflegeeinrichtungen zur Verfügung.
Gesetzliche Grundlage
Meldepflicht gemäß IfSG
Seit Juli 2023 wird dem Gesundheitsamt gemäß § 7 Abs. 1 Nr. 38a IfSG der direkte oder indirekte Nachweis von RSV, soweit er auf eine akute Infektion hinweist, namentlich gemeldet. Dazu gehören auch in ärztlichen Praxen durchgeführte Schnelltests.
Die Meldungen müssen dem Gesundheitsamt spätestens 24 Stunden nach erlangter Kenntnis vorliegen.
In § 8 IfSG werden die zur Meldung verpflichteten Personen benannt (https://www.gesetze-im-internet.de/ifsg/__8.html). In § 9 IfSG ist festgelegt, welche Angaben die namentliche Meldung an das Gesundheitsamt enthalten darf (https://www.gesetze-im-internet.de/ifsg/__9.html).
Übermittlung
Das Gesundheitsamt übermittelt gemäß § 11 Abs. 1 IfSG an die zuständige Landesbehörde nur Erkrankungs- oder Todesfälle und Erregernachweise, die der Falldefinition gemäß § 11 Abs. 2 IfSG entsprechen.
Die vom RKI erstellten Falldefinitionen sind auf den Internetseiten des RKI unter www.rki.de/falldefinitionen veröffentlicht.
Beratung und Spezialdiagnostik
Das RKI führt keine individuelle medizinische Beratung zu Klinik, Therapie oder Impfungen durch. Bitte wenden Sie sich diesbezüglich an Ärztinnen und Ärzte oder Kliniken in Ihrer Nähe, bei denen möglichst eine Spezialisierung für Infektionskrankheiten besteht.
Bezüglich Fragen zu Infektionsschutz und -prävention kontaktieren Sie bitte Ihr zuständiges Gesundheitsamt (https://tools.rki.de/plztool/).
Beratung zur Epidemiologie
Robert Koch-Institut
Abteilung für Infektionsepidemiologie
Fachgebiet 36 - Respiratorisch übertragbare Erkrankungen
Ansprechpartner: Prof. Dr. Walter Haas
Seestraße 10, 13353 Berlin
E-Mail: Kontaktformular
Beratung zur Spezialdiagnostik
Konsiliarlabor für respiratorische Syncytialviren (RSV), Parainfluenzaviren, Metapneumoviren
Robert Koch-Institut
Abteilung für Infektionskrankheiten
Fachgebiet 17 - Influenzaviren und weitere Viren des Respirationstraktes
Seestraße 10, 13353 Berlin
Ansprechpartner: Dr. Janine Reiche (kommissarisch), Dr. Ralf Dürrwald (kommissarisch)
E-Mail: Kontaktformular
Weitere Informationen
RKI: RSV-Infektionen (Respiratorische Synzytial-Viren)
Bundeszentrale für gesundheitliche Aufklärung (BZgA): Erregersteckbrief RSV
Ausgewählte Informationsquellen
- An der Heiden M, Buchholz U, Buda S.: Estimation of influenza- and respiratory syncytial virus-attributable medically attended acute respiratory infections in Germany, 2010/11-2017/18. Influenza Other Respir Viruses. 2019;13(5):517-521, DOI: 10.1111/irv.12666
- Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AMWF): AMWF-Leitlinie 048/012
- Robert Koch-Institut: Informationen zur Aktivität akuter Atemwegserkrankungen (ARE) (URL: http://influenza.rki.de/)
- Berner R, Schwoerer F, Schumacher RF et al.: Community and nosocomially acquired respiratory syncytial virus infection in a German paediatric hospital from 1988 to 1999. Eur J Pediatr 2001; 160:541–547, DOI: 10.1007/s004310100801
- Bont L: Nosocomial RSV infection control and outbreak management. Paediatr Respir Rev (2009):16-17, DOI: 10.1016/S1526-0542(09)70008-9
- Buchholz U, Lehfeld AS, Tolksdorf K et al.: Atemwegsinfektionen bei Kindern und Jugendlichen in Deutschland während der COVID-19-Pandemie. Journal of Health Monitoring. 2023 8(2),
https://www.rki.de/DE/Content/Gesundheitsmonitoring/Gesundheitsberichterstattung/GBEDownloadsJ/Focus/JHealthMonit_2023_02_Atemwegserkrankungen.pdf?__blob=publicationFile - Cai W, Buda S, Schuler E et al.: Risk factors for hospitalized respiratory syncytial virus disease and its severe outcomes. Influenza Other Respir Viruses. 2020;14(6):658-670, http://dx.doi.org/10.25646/6578
- Cai W, Dürrwald R, Biere B et al.: Determination of respiratory syncytial virus epidemic seasons by using 95% confidence interval of positivity rates, 2011-2021, Germany. Influenza Other Respir Viruses. 2022;16(5):854-857, DOI: 10.1111/irv.12996
- Chartrand C, Tremblay N, Renaud C. et al.: Diagnostic Accuracy of Rapid Antigen Detection Tests for Respiratory Syncytial Virus Infection: Systematic Review and Meta-analysis. J Clin Microbiol. 2015;53(12):3738-3749, DOI: 10.1128/JCM.01816-15
- den Hartog G, van Kasteren PB, Schepp RM et al. Decline of RSV-specific antibodies during the COVID-19 pandemic. Lancet Infect Dis. 2023;23(1):23-5, DOI: 10.1016/S1473-3099(22)00763-0
- Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie: Empfehlung zur RSV-Schutzimpfung bei immundefizienten Patientinnen und Patienten mit hämatologischen und/oder onkologischen Erkrankungen. 15. August 2023 (https://www.dgho.de/aktuelles/news/news/2023/download/rsv-impfung-20230815.pdf)
- Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin e.V.: Positionspapier zur RSV-Schutzimpfung bei besonders gefährdeten Patientinnen und Patienten der Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin e.V. 02. November 2023 (https://pneumologie.de/storage/app/media/uploaded-files/2023_RSV-Impfung_DGP.pdf)
- Forster J: Respiratory Syncytial Virus. In: Handbuch Infektionen bei Kindern und Jugendlichen. Hrsg.: Deutsche Gesellschaft für Pädiatrische Infektiologie e.V. (DGPI). 7., vollst. überarb. Aufl., Stuttgart, Thieme-Verlag, 2018, S. 702–706
- Hall CB: Respiratory Syncytial Virus. In: Mandell GL, Bennett JE, Dolin R. Principles and practices of infectious diseases. Churchill Livingstone. 9. Auflage 2019; Kapitel 158
- Jensen TO, Stelzer-Braid S, Willenborg C et al.: Outbreak of respiratory syncytial virus (RSV) infection in immunocompromised adults on a hematology ward. J Med Virol 2016; 88(10):1827–1831, DOI: 10.1002/jmv.24521
- Li Y, Wang X, Blau DM et al.: Global, regional, and national disease burden estimates of acute lower respiratory infections due to respiratory syncytial virus in children younger than 5 years in 2019: a systematic analysis. Lancet 2022;399(10340):2047-2064, DOI: 10.1016/S0140-6736(22)00478-0
- Mesle MMI, Sinnathamby M, Mook P et al.: Seasonal and inter-seasonal RSV activity in the European Region during the COVID-19 pandemic from autumn 2020 to summer 2022. Influenza Other Respi Viruses. 2023;17:e13219, DOI: 10.1111/irv.13219
- Nygaard U, Hartling UB, Nielsen J et al. Hospital admissions and need for mechanical ventilation in children with respiratory syncytial virus before and during the COVID-19 pandemic: a Danish nationwide cohort study. Lancet Child Adolesc Health. 2023;7(3):171-9, DOI: 10.1016/S2352-4642(22)00371-6
- Robert Koch-Institut: Integration von SARS-CoV-2 als Erreger von Infektionen in der endemischen Situation in die Empfehlungen der KRINKO „Infektionsprävention im Rahmen der Pflege und Behandlung von Patienten mit übertragbaren Krankheiten“ Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut. Bundesgesundheitsbl 2023.66:1279–1301. https://doi.org/10.1007/s00103-023-03776-3
- Robert Koch-Institut: Infektionsprävention im Rahmen der Pflege und Behandlung von Patienten mit übertragbaren Krankheiten Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut. Bundesgesundheitsbl 2015.58:1151–1170, https://www.rki.de/DE/Content/Infekt/Krankenhaushygiene/Kommission/Downloads/Infektionspraev_Pflege_Diagnostik_Therapie.pdf
- Robert Koch-Institut: Kommission für Krankenhaushygiene und Infektionsprävention Anforderungen an die Hygiene bei der Versorgung immunsupprimierter Patienten. Bundesgesundheitsbl – Gesundheitsforsch – Gesundheitsschutz 2010; 53:357–388, https://www.rki.de/DE/Content/Infekt/Krankenhaushygiene/Kommission/Downloads/Immunsuppr_Rili.pdf
- RSV Nosocomial Outbreak Investigation Team: Contributing and Terminating Factors of a Large RSV Outbreak in an Adult Hematology and Transplant Unit. PLOS Currents Outbreaks. 2014 Sep 19. Edition 1, DOI: 10.1371/currents.outbreaks.3bc85b2a508d205ecc4a5534ecb1f9be
- Shi T, Denouel A, Tietjen AK et al. Global Disease Burden Estimates of Respiratory Syncytial Virus-Associated Acute Respiratory Infection in Older Adults in 2015: A Systematic Review and Meta-Analysis. J Infect Dis. 2020;222(Suppl 7):S577-S583, DOI: 10.1093/infdis/jiz059
- Simon A, Muller A, Khurana K et al.: Nosocomial infection: A risk factor for a complicated course in children with respiratory syncytial virus infection – Results from a prospective multicenter German surveillance study. Int J Hyg Environ Health 2008; 211:241–250, https://doi.org/10.1016/j.ijheh.2007.07.020
- Simon A, Ammann RA, Wilkesmann A et al.: Respiratory syncytial virus infection in 406 hospitalized premature infants: results from a prospective German multicentre database. Eur J Pediatr 2007; 166:1273–1283, DOI: 10.1007/s00431-007-0426-y
- Teirlinck AC, Broberg EK, Stuwitz Berg A et al: Recommendations for respiratory syncytial virus surveillance at the national level. Eur Respir J. 2021;58(3):2003766, DOI: 10.1183/13993003.03766-2020
- Teirlinck AC, Johannesen CK, Broberg EK et al.: New perspectives on respiratory syncytial virus surveillance at the national level: lessons from the COVID-19 pandemic. Eur Respir J. 2023;61(4):2201569, DOI: 10.1183/13993003.01569-2022
- Wildenbeest JG, Billard MN, Zuurbier RP et al.: The burden of respiratory syncytial virus in healthy term-born infants in Europe: a prospective birth cohort study. Lancet Respir Med. 2023;11(4):341-353, DOI: 10.1016/S2213-2600(22)00414-3
- Koch J, Berner R, Flasche S et al.: Beschluss und wissenschaftliche Begründung zur Empfehlung der STIKO zur spezifischen Prophylaxe von RSV-Erkrankungen mit Nirsevimab bei Neugeborenen und Säuglingen in ihrer 1. RSV-Saison. Epid Bull 2024;26:3-29, DOI: 10.25646/12198
- Falman A, Schönfeld V, Flasche S et al.: Beschluss und Wissenschaftliche Begründung zur Empfehlung der STIKO für eine Standardimpfung gegen Erkrankungen durch Respiratorische Synzytial-Viren (RSV) für Personen ≥ 75 Jahre sowie zur Indikationsimpfung von Personen im Alter von 60 bis 74 Jahren mit Risikofaktoren Epid Bull 2024;32:3-28, DOI: 10.25646/12470
Redaktion der Reihe "RKI-Ratgeber"
Hinweise zur Reihe "RKI-Ratgeber" richten Sie bitte an das RKI, Abteilung für Infektionsepidemiologie (Kontaktformular) oder an die Redaktion des Epidemiologischen Bulletins (Kontaktformular).
nach oben