Mykobakterielle Infektionen: Molekulare Charakterisierung der Erreger und die Immunantwort des Wirtes
Stand: 31.10.2022
Projektleiter: Astrid Lewin und Hubert Schäfer
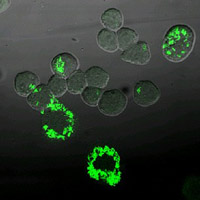
Mit dem gfp-Gen markierte M.bovis BCG in der Maus- Makrophagen Linie J774.
Die Gattung Mycobacterium (M.) umfasst wichtige bakterielle Infektionserreger wie den Tuberkulose-Erreger M. tuberculosis oder den Lepra-Erreger M. leprae. Zu den Mykobakterien zählen aber außerdem ca. 200 Bakterienspezies, die als Nicht-tuberkulöse Mykobakterien (NTM) bezeichnet werden und von denen ca. 40 teilweise ebenfalls schwerwiegende Erkrankungen hervorrufen können. Hierzu zählen neben Lungeninfektionen die Lymphadenitis kleiner Kinder sowie Haut-, Weichteil- und Gelenkinfektionen. Der in Deutschland wichtigste NTM-Erreger ist M. avium subsp. hominissuis, der besonders bei immungeschwächten Personen wie AIDS-Patienten schwerwiegende Infektionen auslösen kann. Ein weiterer Problemkeim, besonders auch bei Patienten mit Mukoviszidose, ist das sehr schwer zu behandelnde M. abscessus.
Die Zahl der durch NTM hervorgerufenen Erkrankungen hat in den letzten zwei Jahrzehnten in den industrialisierten Ländern einschließlich Deutschland zugenommen. Deshalb besteht sowohl hinsichtlich der Pathogenität der Erreger als auch zur Verbesserung diagnostischer und therapeutischer Ansätze bei diesen Infektionen erheblicher Forschungsbedarf.
Im Rahmen dieses Projektes sollen einerseits die Wirkmechanismen identifiziert und charakterisiert werden, die es Mykobakterien ermöglichen, den Abwehrmechanismen des Immunsystems zu entkommen. Hierzu vergleichen wir die genetische Struktur unterschiedlicher Erreger, identifizieren Virulenzgene und untersuchen deren Auswirkungen auf die Interaktion mit Wirtszellen. Ein besonderes Schwergewicht unserer Arbeiten liegt auf der Charakterisierung von Erregern der Arten M. avium und M. abscessus, die besonders bei immungeschwächten Personen und bei Personen mit Mukoviszidose schwer zu behandelnde Lungeninfektionen verursachen.
In unseren Arbeiten zu dem Erreger M. avium liegt ein weiterer Fokus auf der Untersuchung der genetischen Diversität und ihrer Bedeutung für die Virulenz sowie die Identifizierung von Infektionsquellen.
Im Mittelpunkt der Arbeiten zu dem Erreger M. abscessus steht die molekulare Surveillance der Erregerpopulation bei Patienten mit Mukoviszidose im Vordergund. Hierbei sollen Infektionsquellen und Transmissionen aufgedeckt werden, neue Resistenz- und Virulenzgene identifiziert werden und die Anpassung der Erreger an den Wirt bei chronisch persistierenden Infektionen beschrieben werden.
Nicht-tuberkulöse Mykobakterien sind in der Lage, sowohl im Patienten als auch in der Umwelt oder in/auf medizinischen Geräten Biofilme auszubilden. Diese Biofilme verleihen ihnen eine erhöhte Widerstandsfähigkeit sowohl gegen Desinfektionsmaßnahmen als auch gegen Antibiotikaeinsatz. In Kooperation mit dem Fachgebiet 14 untersuchen wir die genetischen Grundlagen der Biofilmbildung von Nicht-tuberkulösen Mykobakterien und die Auswirkung der Biofilmbildung auf die Resistenz gegen Desinfektionsverfahren und Antibiotikaeinsatz.
Auf der anderen Seite der Interaktion zwischen Krankheitserreger und Wirt versuchen wir die Immunmechanismen zu identifizieren und zu charakterisieren, die bei der Abwehr mykobakterieller Infektionen wirksam werden. Hierzu werden die durch eine M. avium-Infektion hervorgerufenen Immunreaktionen charakterisiert. Parallel dazu sollen diejenigen Effektormechanismen identifiziert werden, die nach Immunisierung mit dem Impfstamm BCG (Bacille Calmette Guérin) einen gewissen Schutz vor Infektionen mit Mykobakterien verleihen.
In einem weiteren Ansatz versuchen wir spezifisch die Proteine von Mycobacterium avium hominissuis zu identifizieren, die bei Infektion eine Immunantwort auslösen, also als Antigene wirken. Die Kenntnis dieser Antigene kann dann zur Verbesserung diagnostischer Maßnahmen oder zur Entwicklung neuer Impfstoffe beitragen.
Mitarbeiter:
Elisabeth Kamal, Barbara Kropp
Teilprojekte:
- Molekulare Surveillance von Nicht-tuberkulösen Mykobakterien aus Patienten mit Mukoviszidose
- Vergleichende Analyse der Genomstruktur von M. avium-Isolaten und M. abscessus-Isolatenaus Patienten und aus der Umwelt
- Untersuchung der Interaktion unterschiedlicher M. avium- und M. abscessus-Isolate mit humanen Zellen
- Identifizierung und Charakterisierung neuer Virulenz- und Resistenzfaktoren von M. avium und M. abscessus
- Genetische Grundlagen der Biofilmbildung von Nicht-tuberkulösen Mykobakterien und ihre Auswirkungen aus Desinfektionsverfahren und Antibiotikatherapie (Kooperation mit FG 14)
- Identifizierung immunogener Proteine aus Mycobacterium avium
- Charakterisierung von Effektormechanismen bei der Immunantwort gegen Mykobakterien
