Fradin C, Poulain D, Jounault T (2000): Beta-1,2-linked oligomannosides from Candida albicans bind to a 32-kilodalton macrophage membrane protein homologous to the mammalian lectin galectin-3
Infect. Immun. 68 (8): 4391-4398.
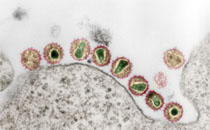
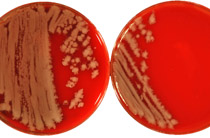
Beta-1,2-linked oligomannoside residues are present, associated with mannan and a glycolipid, the phospholipomannan, at the Candida albicans cell wall surface. Beta-1,2-linked oligomannoside residues act as adhesins for macrophages and stimulate these cells to undergo cytokine production. To characterize the macrophage receptor involved in the recognition of C. albicans beta-1,2-oligomannoside we used the J774 mouse cell line, which is devoid of the receptor specific for alpha-linked mannose residues. A series of experiments based on affinity binding on either C. albicans yeast cells or beta-1,2-oligomannoside-conjugated bovine serum albumin (BSA) and subsequent disclosure with biotinylated conjugated BSA repeatedly led to the detection of a 32-kDa macrophage protein. An antiserum specific for this 32-kDa protein inhibited C. albicans binding to macrophages and was used immunoprecipitate the molecule. Two high-pressure liquid chromatography-purified peptides from the 32-kDa tryptic digest showed complete homology to galectin-3 (previously designated Mac-2 antigen), an endogenous lectin with pleiotropic functions which is expressed in a wide variety of cell types with which C. albicans interacts as a saprophyte or a parasite.