Hengel H, Reusch U, Geginat G, Holtappels R, Ruppert T, Hellebrand E, Koszinowski UH (2000): Macrophages escape inhibition of major histocompatibility complex class I-dependent antigen presentation by cytomegalovirus
J. Virol. 74 (17): 7861-7868.
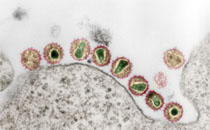
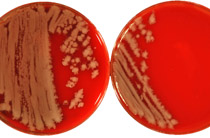
The mouse cytomegalovirus (MCMV) m152- and m06-encoded glycoproteins gp40 and gp48, respectively, independently downregulate major histocompatibility complex (MHC) class I surface expression during the course of productive MCMV infection in fibroblasts. As a result, presentation of an immediate-early protein pp89-derived nonapeptide to H-2L(d)-restricted CD8(+) cytotoxic T cells is completely prevented in fibroblasts. Here we demonstrate that MCMV-infected primary bone marrow macrophages and the macrophage cell line J774 constitutively present pp89 peptides during permissive MCMV infection to cytotoxic T lymphocytes (CTL). In contrast to fibroblasts, expression of the m152 and m06 genes in macrophages does not affect surface expression of MHC class I. Assessment of pp89 synthesis and quantification of extracted peptide revealed a significantly higher efficiency of macrophages than of fibroblasts to process pp89 into finally trimmed peptide. The yield of pp89 peptide determined in MCMV-infected tissues of bone marrow chimeras confirmed that bone marrow-derived cells represent a prime source of pp89 processing in parenchymal organs. The finding that macrophages resist the viral control of MHC I-dependent antigen presentation reconciles the paradox of efficient induction of CMV-specific CD8(+) CTL in vivo despite extensive potential of CMVs to subvert MHC class I.